morild er luminescens, der opstår når energi leveres af elektromagnetisk stråling, normalt ultraviolet lys. Energikilden sparker en elektron af en atom fra en lavere energitilstand til en "ophidset" højere energitilstand; så frigiver elektronet energien i form af synligt lys (luminescens), når den falder tilbage til en lavere energitilstand.
Key takeaways: Phosphorescence
- Phosphorescence er en type fotoluminescens.
- I phosphorescens absorberes lys af et materiale, hvorved energiniveauet for elektroner stødes op i en ophidset tilstand. Lysets energi stemmer imidlertid ikke helt overens med energien i tilladte ophidsede tilstande, så de absorberede fotos sidder fast i en triplet tilstand. Overgange til en lavere og mere stabil energitilstand tager tid, men når de forekommer, frigives lys. Fordi denne frigivelse sker langsomt, ser det ud til, at et fosforescerende materiale lyser i mørke.
- Eksempler på phosphorescerende materialer inkluderer glød-i-mørke stjerner, nogle sikkerhedsskilte og glødende maling. I modsætning til phosphorescerende produkter holder fluorescerende pigmenter med at glødes, når lyskilden er fjernet.
- Selvom den er navngivet efter den grønne glød fra fosforelementet, gløder fosfor faktisk på grund af oxidation. Det er ikke phosphorescerende!
Enkel forklaring
Phosphorescens frigiver langsomt den lagrede energi over tid. Grundlæggende "fyldes" phosphorescerende materiale ved at udsætte det for lys. Derefter lagres energien i et tidsrum og frigives langsomt. Når energien frigives umiddelbart efter absorbering af den hændende energi, kaldes processen fluorescens.
Kvantemekanik Forklaring
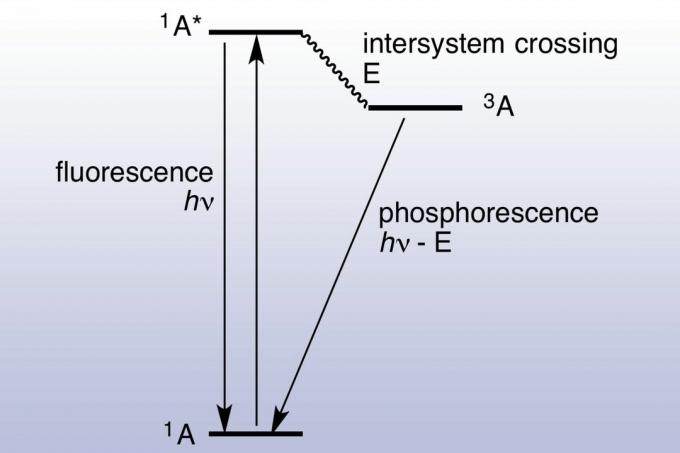
I fluorescens absorberer og udsender en overflade næsten øjeblikkeligt et foton (ca. 10 nanosekunder). Fotoluminescens er hurtig, fordi energien i de absorberede fotoner matcher energitilstander og tilladte overgange af materialet. Fosfororescens varer meget længere (millisekunder op til dage), fordi den absorberede elektron krydser til en ophidset tilstand med højere spin-multiplicitet. De ophidsede elektroner bliver fanget i en tripletilstand og kan kun bruge "forbudte" overgange til at falde til en singlet tilstand med lavere energi. Kvantemekanik tillader forbudt overgang, men de er ikke kinetisk gunstige, så det tager længere tid at forekomme. Hvis der optages nok lys, bliver det lagrede og frigjorte lys tilstrækkeligt betydningsfuldt til, at materialet ser ud til at "gløde i Af denne grund ser phosphorescerende materialer, som fluorescerende materialer, meget lyse ud under et sort (ultraviolet) lys. Et Jablonski-diagram bruges ofte til at vise forskellen mellem fluorescens og phosphorescens.
Historie
Undersøgelsen af phosphorescerende materialer stammer tilbage til mindst 1602, da italienske Vincenzo Casciarolo beskrev en "lapis solaris" (solsten) eller "lapis lunaris" (månesten). Opdagelsen blev beskrevet i filosofiprofessor Giulio Cesare la Gallas bog fra 1612 De Phenomenis i Orbe Lunae. La Galla rapporterer, at Casciarolo's sten udsendte lys på den, efter at den var blevet forkalket gennem opvarmning. Den modtog lys fra solen og udsendte derefter (som månen) lys i mørket. Stenen var uren barit, skønt andre mineraler også udviser phosphorescens. De inkluderer nogle diamanter (kendt af den indiske konge Bhoja allerede i 1010-1055, genopdaget af Albertus Magnus og igen genopdaget af Robert Boyle) og hvid topas. Kineserne værdsatte især en type fluorit kaldet chlorophan, der ville udvise luminescens fra kropsvarme, udsættelse for lys eller blive gnidet. Interesse for arten af fosforescens og andre typer luminescens førte til sidst til opdagelsen af radioaktivitet i 1896.
Materialer
Udover et par naturlige mineraler produceres fosforescens af kemiske forbindelser. Sandsynligvis er den bedst kendte af disse zinksulfid, der er blevet brugt i produkter siden 1930'erne. Zinksulfid udsender normalt en grøn phosphorescens, skønt fosfor kan tilsættes for at ændre lysets farve. Fosfor absorberer det lys, der udsendes ved phosphorescens, og frigiver det derefter som en anden farve.
For nylig anvendes strontiumaluminat til phosphorescens. Denne forbindelse glider ti gange lysere end zinksulfid og opbevarer også sin energi meget længere.
Eksempler på phosphorescens
Almindelige eksempler på fosforescens inkluderer stjerner, som mennesker lægger på soveværelsesvægge, der gløder i timevis efter at lysene er slukket og maling, der bruges til at fremstille glødende stjernemalerier. Selvom elementet fosfor lyser grønt, lyset frigøres fra oxidation (kemiluminescens) og er ikke et eksempel på phosphorescens.
Kilder
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Selvlysende materialer" i Ullmanns encyklopædi for industriel kemi. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Kemiluminescens og bioluminescens: fortid, nutid og fremtid. Royal Society of Chemistry.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Mikrobølge-syntese af en langvarig fosfor. J. Chem. educ. 86. 72-75. doi: 10.1021 / ed086p72