Bufferløsninger er vandbaserede væsker, der inkluderer både en svag syre og dens konjugatbase. På grund af deres kemi kan bufferopløsninger holde pH (surhedsgrad) på et næsten konstant niveau, selv når der sker kemiske ændringer. Puffersystemer forekommer i naturen, men de er også ekstremt nyttige i kemi.
Anvendelser til bufferløsninger
I organiske systemer holder naturlige bufferopløsninger pH på et konstant niveau, hvilket gør det muligt for biokemiske reaktioner at forekomme uden at skade organismen. Når biologer studerer biologiske processer, skal de opretholde den samme konsistente pH; for at gøre det brugte de forberedte pufferopløsninger. Bufferopløsninger blev først beskrevet i 1966; mange af de samme buffere bruges i dag.
For at være nyttigt skal biologiske buffere opfylde flere kriterier. De bør specifikt være vandopløselige, men ikke opløselige i organiske opløsningsmidler. De skal ikke være i stand til at passere gennem cellemembraner. Derudover skal de være ikke-toksiske, inerte og stabile i alle eksperimenter, som de anvendes til.
Bufferopløsninger forekommer naturligt i blodplasma, hvorfor blod opretholder en konstant pH mellem 7,35 og 7,45. Bufferopløsninger bruges også i:
- gæringsprocesser
- døende stoffer
- kemisk analyse
- kalibrering af pH-målere
- DNA-ekstraktion
Hvad er Tris Buffer Solution?
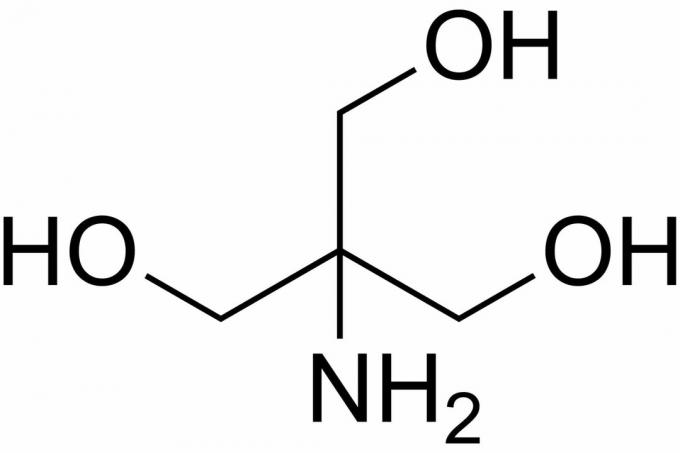
Tris er en forkortelse for tris (hydroxymethyl) aminomethan, en kemisk forbindelse, der ofte bruges i saltvand, fordi det er isotonisk og ikke-toksisk. Fordi det har en Tris, har en pKa på 8,1 og et pH-niveau mellem 7 og 9, bruges Tris-pufferopløsninger også ofte i en række kemiske analyser og procedurer, herunder DNA-ekstraktion. Det er vigtigt at vide, at pH i trisbufferopløsning ændrer sig med temperaturen på opløsningen.
Sådan klargøres Tris Buffer
Det er let at finde kommercielt tilgængelig trisbuffer-løsning, men det er muligt at fremstille det selv med det passende udstyr.
Materialer:
Beregn mængden af hvert element, du har brug for, baseret på den molære koncentration af den ønskede opløsning og den mængde buffer, du har brug for.
- tris (hydroxymethyl) aminomethan
- destilleret deioniseret vand
- HCI
Procedure:
- Start med at bestemme hvilken koncentration (molariteten) og volumen af den Tris-buffer, du vil oprette. For eksempel varierer Tris-bufferopløsningen anvendt til saltvand fra 10 til 100 mM. Når du har besluttet, hvad du laver, skal du beregne antallet af mol Tris, der kræves, ved at multiplicere den molære koncentration af puffer med volumenet af den puffer, der laves. (mol Tris = mol / L x L)
- Derefter bestemmes hvor mange gram Tris dette er ved at multiplicere antallet af mol med molekylvægten af Tris (121,14 g / mol). gram Tris = (mol) x (121,14 g / mol)
- Opløs Tris i det destillerede deioniserede vand, 1/3 til 1/2 af det ønskede slutvolumen.
- Bland HCI (f.eks. 1 M HCI) indtil pH-meter giver dig den ønskede pH-værdi for din Tris-bufferopløsning.
- Fortynd bufferen med vand for at nå det ønskede slutvolumen af opløsningen.
Når opløsningen er blevet forberedt, kan den opbevares i måneder i en steril placering ved stuetemperatur. Tris-bufferopløsningens lange holdbarhed er mulig, fordi opløsningen ikke indeholder proteiner.